Страница: 5/8
II. Реакции транскарбоксилирования, протекающие без распада АТФ, при которых карбоксилирование одного субстрата осуществляется при одновременно протекающем декарбоксилировании другого соединения:
R1—COO- + R2H![]() R1H + R2— COO-
R1H + R2— COO-
Поскольку все приведенные реакции являются обратимыми, возможен обратимый биосинтез АТФ. Во всех этих случаях имеет место включение С02 в реактивное α-подожение ацил-КоА или винилгомоло-гичное ему положение (при карбо^силировании β-метилкротонил-КоА).
К началу 60-х год5В были выделены и изучены карбоксилазы, осуществляющие указанные превращения —В 1960 г. установлено участие биотина в реакции транскарбоксилирования при исследовании синтеза пропионовои кислоты
СНз—СН—СО~S—КоА + СНз—СО—СООН
![]()
![]()
СООН
![]() СНз-СНа—СО~S-КоА
+ НООС-СН2—СО—СООН
СНз-СНа—СО~S-КоА
+ НООС-СН2—СО—СООН
Биотиновые ферменты представляют собой олигомеры с большим молекулярным весом (порядка 700000) и, как правило, содержат 4 моля связанного биотина на 1 моль фермента, поэтому кажется вероятным, что они состоят из 4 субъединиц с молекулярным весом 175000, каждая из которых содержит одну молекулу биотина.
В работах Lynen (1964) расшифрован механизм участия биотина в реакциях карбексилирования. Установлено, что реакции карбоксилирования являются двухстадийными. Первая стадия сводится к образованию «активной С02» в форме С02~биотинфермента:
АТФ + Н С0-2+ биотинфермент
![]() АДФ + Фнеорг. + С02~биотинфермент.
АДФ + Фнеорг. + С02~биотинфермент.
Вторая стадия заключается в переносе «активной С02» на акцептор:
С02~биотинфермент + R2H
![]() биотинфермент + R2—
С00-
биотинфермент + R2—
С00-
Аналогичный двух стадийный механизм предложен и для реакций транскарбоксилирования:
R1 —С00- + биотинфермент
![]() С02 ~биотинфермент
R2H;
С02 ~биотинфермент
R2H;
С02~биотинфермент + R2H![]() R2—
С00- + биотинфермент.
R2—
С00- + биотинфермент.
После установления существования «активной С02» в виде С02~биотинфермента установлен характер связи между С02 и биотином. Этому способствовало открытие того факта, что β-метилкротонил-КоА-карбоксилаза способна карбоксилировать свободный биотин, переводя его в карбоксибиотин. В дальнейшем меченый карбоксибиотип был выделен в опытах с С14-бикарбонатом и идентифицирован как Г-М-карбоксибиотин. Его структура была подтверждена химическим синтезом. К атому времени уже было известно, что в биотиновых ферментах карбоксильная группа биотина соединена с ε-NH2-группой лизина ферментного белка ковалентной связью. На основании этих данных предложена структура С02~биотинфермента.
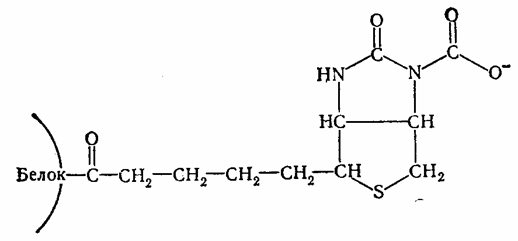
Эта структура получила ряд экспериментальных подтверждений и в настоящее время является общепринятой для всех биотиновых ферментов. Реакционная способность углекислоты, связанной с биотином, находит выражение в энергетических взаимоотношениях. Величина свободной энергии распада С02~биотинфермента равна 4,74 ккал/моль, что дает основание причислить С02~биотинфермента к «богатым энергией» соединениям.
Исключительно большой интерес представляет совершенно неизученная проблема регуляции активности биотинсодержащих ферментов и организме. В этой связи особенно важны исследования по биосинтезу молекулы биотина и образованию холоферментов из биотина и соответствующего ферментного белка. Данные по первому вопросу изложены в разделе «Биосинтез». Что касается образования холофермента, то можно считать установленным, что во всех биотиновых ферментах био-тнн связан с ε-аминогруппой лизина. Этот способ связи экспериментально доказан почти для всех карбоксилаз и метилмалонил-КоА-оксалоаце-таттранскарбоксилазы. Недостаточные по биотину клетки Propionibacterium shcemanii содержат апофермент и специфическую синтетазу, которая катализирует при использовании АТФ соединение биотина с апоферментом, приводящее к образованию активного холофермента траискарбокснлазы. Необходимыми кофакторами этой реакции являются АТФ и Mg2+. При использовании очищенных ферментов удалось доказать, что образование холотранскарбоксилазы происходит в два этапа, причем промежуточным соединением является биотиниладенилат (R-CO-5'-AMФ):
Mg2+
I. АТФ + R— С02Н + синтетаза![]() R-СО-5’-
АМФ - синтетаза + пирофосфат
R-СО-5’-
АМФ - синтетаза + пирофосфат
(биотин
![]() II. R-СО-5’-
АМФ - синтетаза + Н2М-фермент R-CO-NH-фермент +
II. R-СО-5’-
АМФ - синтетаза + Н2М-фермент R-CO-NH-фермент +
+5’-AMФ+cинтeтaзa.
Синтетический биотиниладенилат обладает способностью заменить смесь АТФ, MgCl и биотина при синтезе холофермента (Lynen, 1964). Позже было установлено, что образование других холоферментов протекает аналогичным образом. Все известные ферментативные реакции, для которых установлено участие биотина в качестве кофермента, являются процессами переноса углекислоты. По-видимому, в обратимом присоединении и отдаче СО; и состоит исключительная функция этого витамина в обмене веществ. Однако при биотиновой недостаточности нарушаются очень многие реакции обмена в интактном организме. Так, - биотин вовлечен в биосинтез белков, дезаминирование аспартата, серина и треонина у бактерий, обмен триптофана, жиров и углеводов, синтез пуринов, образование мочевины у животных и др. Природа участия биотина во многих из этих реакций остается неясной. Все перечисленные процессы имеют одну общую черту: при изучении in vitro они не тормозятся авидином. На основании этих данных считается, что биотин оказывает.непрямое действие на указанные превращения, которые катализируются ферментами, не содержащими этого витамина.
Ввиду чрезвычайной важности нeкоторых из этих реакций для жизне-деятельности организма необходимо рассмотреть их. Рядом авторов отмечено, что при недостаточности биотина в рационе крыс снижается включение в белок меченых аминокислот. Так, включение (С14-метионина, С14-лейцина и С14-лизина в тканевые белки снижается на 20—40% причем недостаточность биотина влияет на стадию образования амино-ацил-транспортной РНК. Препараты тРНК из печени нормальных крыс включают значительно больше меченых аминокислот, чем препараты печени авитаминозных животных (Dakshinainurti, Misty, 1964). Еще ранее было установлено, что у авитаминозных животных нарушается синтез амилазы в поджелудочной железе и сывороточного альбумина в печени, причем однократное введение 100 мкг биотина восстанавливает способность тканей к синтезу указанных белков. Добавление in vitro α-кетоглутарата и фумарата также восстанавливает образование амилазы и сывороточного альбумина (А. А. Познанская, 1957).
Эти данные показали, что биотин не принимает прямого участия в синтезе белка de novo, а его влияние на этот процесс, по-видимому, определяется вовлечением биотина в синтез субстратов трикарбонового цикла. Такое предположение нашло подтверждение в опытах на цыплятах: скармливание сукцината авитаминозным птицам восстанавливало до нормы включение аминокислот в тканевые белки и РНК. Так как образование С4-дикарбоновых кислот в организме животных протекает через фиксацию СО2, осуществляемую биотиновыми ферментами, то становятся ясными причины нарушения синтеза белка при биотиновой недостаточности. В организме авитаминозных цыплят значительно снижены скорость окисления глюкозы до СО2 и включение ее в гликоген печени. Имеются указания на снижение глюкокиназной активности при недостаточности биотина, хотя витамин не был обнаружен в препаратах кристаллического фермента. Возможно, что участие биотина в обмене. углеводов является непрямым. В результате нарушения утилизации глюкозы в организме животных при исключении биотина из корма нарушается превращение D-глюкозы в L-аскорбиновую кислоту.
При недостаточности биотина содержание липидов в печени животных снижается на 30°/о, что обусловлено снижением синтеза жирных кислот. Отсутствие биотина в корме цыплят приводит к повышению содержания триглицеридов, пальмитиновой и пальмитолеиновой кислот в печени, а также соотношения жирных кислот СО16, СО18 соотношение между насыщенными жирными кислотами при этом снижается. Включение введенных СО14-стеариновой и СО14-пальмитиновой кислот в фосфолипиды значительно повышается при недостаточности биотина, а включение их в триглицериды—снижается. При этом общее количество жирных кислот по сравнению с контролем понижено. В печени авитаминозных крыс снижено включение СО14-ацетата в липиды и наблюдается большее содержание ненасыщенных жирных кислот СО16:1 и СО18:2, тогда как уровень стеариновой кислоты снижен. Исключение биотина из корма крыс в течение 60 дней приводит к значительному снижению уровня цитидиловых, адениловых и гуаниловых нуклеотидов в печени. Содержание уридиловых нуклеотидов при этом почти не изменяется, а инозиловых — немного повышается. В то же время отсутствие биотина в рационе не влияет на содержание РНК и ДНК, а также на включение в них Р32, введенного внутрибрюшинно в виде Na2HP32O4.
Наконец, в гомогенатах печени авитаминозных крыс резко снижено образование цитруллина, которое полностью восстанавливается через 24 часа после введения животным биотина. Однако биотин не обнаружен в препаратах ферментов, участвующих в синтезе мочевины (карбамилфосфатсинтетаза, орнитинтранскарбамилаза и др.) и, по-видимому, в данном случае оказывает непрямое действие на эту реакцию.
6.1 Взаимодействие с другими витаминами. Установлена связь биотина с другими витаминами, в частности с фолиевой кислотой, витамином B12 - аскорбиновой кислотой, тиамином и пантотеновой кислотой. 0собенно тесные взаимоотношения существуют между биотином и фолиевой кислотой. Сначала было показано, что при недостатке биотина в печени крыс значительно снижено общее содержание веществ, обладающих активностью фолиевой кислоты. и что биотин стимулирует биосинтез этого витамина с флорой. Позднее было установлено, что у биотинавитаминозных крыс значительно снижено содержание коферментны.х форм фолиевой кислоты, а именно N5 и N10-формилтетрагидро-фолатов, тетрагидрофолата, N5_ и N10_ формилтетрагидроптероилглутаминовых кислот. Биотин стимулирует синтез метионина из серина и гомоцистеина и процессы метилирования вообще, способствуя накоплению коферментных форм фолиевой кислоты. Таким образом, при недостаточности биотина нарушена утилизация организмом фолиевой кислоты и превращение ее в активные коферментные формы. По-видимому, биотин принимает непосредственное участие в ферментативных процессах превращения фолиевой кислоты в ее коферментные производные (Marchetti e. а., 1966). Биотин благоприятно влияет на общее состояние организма и сохранение аскорбиновой кислоты в тканях цинготных морских свинок. В свою очередь аскорбиновая кислота замедляет, хотя и не предотвращает развитие авитаминоза биотина у крыс. При недостаточности биотина снижается содержание тиамина в печени, селезенке,. почках и мозге животных. У крыс, содержавшихся на рационе, лишенном биотина, содержание витамина B12 было выше, чем у контрольных животных, получавших биотин. Эти два витамина тесно связаны между собой в обмене пропионовой кислоты у микроорганизмов и животных. Существует тесная связь между биосинтезом биотина и пантотеновой кислоты у микроорганизмов и зеленых растений (В. В. Филиппов, 1962). Биотин облегчает симптомы пантотеновой недостаточности и, наоборот, пантотеновая кислота смягчает проявление авитаминоза биотина.
7. Потребность организма в биотине.
Биотин необходим для человека, животных, растений и большого числа микроорганизмов. Он является фактором роста для многих штаммов, а также многих грибов и бактерий. Однако некоторые дрожжи, грибы и бактерии способны его синтезировать. Потребность в биотине у птиц и животных покрывается за счет синтеза его бактериями желудочно-кишечного тракта. У коров, овец и лошадей, содержащихся на обычном рационе, практически исключена недостаточность биотина. У свиней и птиц недостаточность биотина может создаваться при использовании кормов, бедных витаминами.
Потребность в биотине у человека покрывается за счет синтеза его микрофлорой кишечника, поэтому ее трудно оценить. С известной долей приближения можно считать, что (минимальной ежедневной дозой биотина для животных и человека являются следующие величины (Gyorgy, 1954): для человека— 150—200 мкг, обезьян—20 мкг, крыс— 0,5—3 мкг, цыплят — 0,65—1 мкг, свинец — 100 мкг.
В период беременности и лактации Потребность в биотине у женщин повышается до 250— 300 мкг в день. По другим данным, потребность в биотине значительно ниже и составляет для взрослого человека 30— 40 мкг в сутки.
7.1 Проявление недостаточности биотина
Наиболее подробно недостаточность биотина изучена в опытах на крысах и цыплятах при скармливании рационов с большим содержанием сырого яичного белка. Биотиновый авитаминоз у животных характеризуется прекращением роста и падением веса тела (до 40%), покраснением и шелушением кожи, выпадением шерсти или перьев, образованием красного отечного ободка вокруг глаз в виде «очков», атактической походкой, отеком лапок и типичной позой животного с согбенной (кенгу-руподобной) спиной. Дерматит, который развивается у животных при недостаточности биотина, может быть охарактеризован как себорея десквамационного типа, сходная с той, которая наблюдается у детей. У крыс авитаминоз биотина развивается через 4—5 недель скармливания опытного рациона, а у цыплят первые признаки авитаминоза появляются через 3 недели.
Помимо внешних признаков, биотиновый авитаминоз вызывает глубокие морфологические изменения в тканях и органах, а также нарушения в обмене веществ. Известны изменения в зобной железе, коже и мышцах крыс. Характерны обильный гиперкератоз, акантез и отеки. Разрушенные волосяные стволы перемешаны с гиперкератозными пластинками. Установлено расширение волосяных сумок, отверстия которых закупорены гиперкератозным материалом. В последней фазе развития авитаминоза наблюдается атрофия жира в гиперкератозных пластинках. Недостаток биотина в рационе крыс приводит к уменьшению его содержания в тканях. В печени и мышцах количество витамина снижается в 5 раз, а в мозговой ткани—на 15%. В крови авитаминозных крыс накапливается пировиноградная кислота, развивается ацидоз и снижается концентрация сахара. При этом глюкозурия не наблюдается, но уменьшается содержание редуцирующих Сахаров в печени при нормальном содержании их в мышцах; у животных развивается креа-тинурия.
Человек полностью удовлетворяет свою потребность в биотине за счет синтеза его микрофлорой кишечника, поэтому гиповитаминоз можно получить только в эксперименте. Экспериментальную недостаточность биотина у человека наблюдали Sydenstricker и соавторы (1942) путем включения в диету ежедневно 200 г сырого яичного белка. Через 3 недели появилось шелушение кожи без зуда. На 7—8-й день развилась пепельная бледность кожи и началась атрофия вкусовых сосочков языка. Позднее появились мышечные боли, повышенная чувствительность, болезненные ощущения, вялость, сонливость, тошнота и потеря аппетита. В крови уменьшилось содержание эритроцитов и холестерина. Выделение биотина с мочой снизилось в 7—8 раз против нормы (с 29— 52 до 3,5—7,3 мкг в сутки). Введение 150 мкг биотина уже на 3—4-й день устраняло депрессию, мышечные боли и восстанавливало аппетит.
Таким образом, недостаточность биотина у человека в первую очередь вызывает поражения кожи. Более тяжелые проявления требуют, по-видимому, большей длительности авитаминоза.
8. Профилактическое и лечебное применение биотина.
В настоящее время применение биотина в клинике с лечебной и профилактической целью изучено недостаточно. Большое значение биотина для нормального состояния кожных покровов привело к попыткам лечения биотином ряда кожных заболеваний. Биотин показан при себорейном дерматите у грудных детей, связанном, возможно, с явлениями недостаточности этого витамина. Заболевание излечивается при ежедневном введении 5—10 мкг биотина в течение 4 недель. Отмечен успех при длительном применении биотином в тех случаях дескваматозной эритродермии, когда недостаточность биотина была в числе причин заболевания. Лечебная доза биотина составляет 150—300 мкг в сутки; вводится он-парентерально.
Г. И. Бежанов в 1966 г. сообщил о применении биотина в комплексной терапии псориаза. Наблюдения, проведенные за большой группой больных, показали, что биотин проявлял противозудный эффект, а сочетание биотина с фумаратом, витаминами группы В и бальнеотерапией потенцированный и более быстрый клинический эффект. В процессе лечения у значительного большинства больных рассасывался инфильтрат, уменьшалось или полностью прекращалось шелушение. Автор рекомендует применять биотин в комплексном лечении псориаза.
В последние годы появился ряд сообщений о целесообразности применения фармакологических доз биотина п комплексной терапии атеросклероза и гипертонической болезни.. Эти данные представляют особый интерес в связи с участием биотина в синтезе холестерина.
О. К. Докусова и А. Н. Климов в 1967 г. сообщили о предотвращении биотином экспериментального атеросклероза у кроликов при скармливании больших доз холестерина. Введение биотина в количестве 400 мкг в день предупреждало развитие атеросклероза. Содержание холестерина, β -липопротеидов и фосфолипидов в стенке аорты животных, получавших холестерин и биотин, не отличалось от содержания этих компонентов в аорте здоровых кроликов, тогда как в аорте животных, получавших холестерин без биотина, содержание холестерина и β-липопро-теидов было резко повышено. Авторы считают, что снижение содержания холестерина вызвано окислением его в печени. В настоящее время известно, что пропионат является основным трехуглеродным фрагментом, отщепляющимся от боковой цепи холестерина на первых этапах окисления холестерина в желчные кислоты. Можно предположить, что стимуляция окисления холестерина биотином связана с активацией окисления пропионовой кислоты (через образование янтарной кислоты путем кар-боксилирования пропионовой кислоты), поскольку пропионил-КоА-кар-боксилаза является биотинсодержащим ферментом.
В. Д. Устиловский и др. (1967) сообщил, что после 7-дневного введения внутрь фармакологических доз биотина у больных атеросклерозом, отмечалось статистически достоверное снижение содержания общего, холестерина и β -липопротеидов в крови, тогда как у здоровых людей биотин не влиял на изучаемые показатели. У больных атеросклерозом и гипертонической болезнью применение фармакологических доз биотина приводит к значительному снижению выведения с мочой тиамина и аскорбиновой кислоты (М. А. Лис, 1967; Д. П. Калкун, 1967).
Таким образом, биотин способствует усвоению этих витаминов в организме больных. Учитывая благоприятное влияние биотина на ряд показателей липидного обмена у больных атеросклерозом и гипертонической болезнью, а также повышение усвоения тиамина и аскорбиновой кислоты, авторы рекомендуют применять биотин при этих заболеваниях в дозе 1 мг в день внутрь в комплексной терапии,
С возрастом в крови людей снижается содержание пантотеновой кислоты, витамина В6 и биотина (В. И. Титов, 1966). У больных гипертонией и атеросклерозом в возрасте 80—88 лет содержание биотина было в 2,4 раза меньше, чем у здоровых молодых людей. Установлено снижение содержания биотина в крови больных, жаловавшихся на слабость, недомогание и легкую утомляемость. Автор рекомендует применять пантотеновую кислоту, витамин В6 и биотин при преждевременной старости для устранения явлений гиповитаминоза и связанного с ним нарушением обмена веществ. Некоторыми исследователями обнаружено высокое содержание биотина в тканях ряда раковых опухолей, что привело к попыткам воздействовать на развитие рака путем вызывания биотиновой недостаточности. Однако эти попытки не дали положительных результатов.
Таким образом, сейчас накапливаются данные, позволяющие рекомендовать применение биотина при некоторых болезнях кожи, нарушениях жирового обмена и сердечно-сосудистых заболеваниях. Однако для более широкого использования биотина в клинике необходимо дальнейшее изучение как его физиологического действия, так и показаний к лечебному применению.
Тиамин
Исторические сведения
Первые упоминания о заболевании (какке, бери-бери), известном сейчас как проявление недостаточности тиамина, встречаются в древних медицинских трактатах, дошедших до нас из Китая, Индии, Японии (Bicknell, Prescott, 1953; Inouye, Katsura, 1965). К концу прошлого столетия клинически уже различали несколько форм этой патологии, но только Takaki (1887) связал заболевание с какой-то, как он тогда полагал, недостаточностью азотсодержащих веществ в пищевом рационе. Более определенные представления были у голландского врача С. Eijkman (1893—1896), обнаружившего в рисовых отрубях и в некоторых бобовых растениях неизвестные тогда факторы, предупреждавшие развитие или излечивавшие бери-бери. Очисткой этих веществ занимались затем Funk (1924), впервые предложивший сам термин «витамин», и ряд других исследователей (Wuest, 1962). Извлеченное из естественных источников активное вещество только в 1932 г. было охарактеризовано общей эмпирической формулой, а затем (1936) успешно синтезировано. Еще в 1932 г. высказывалось предположение о роли витамина в одном из конкретных процессов обмена веществ—декарбоксилировании пировиноградной кислоты, но лишь в 1937 г. (Lohman, Schuster) стала известна коферментная форма витамина—тиаминдифос-фат (ТДФ). Коферментные функции ТДФ в системе декарбоксилирования ct-кето-кислот долгое время представлялись почти единственными биохимическими механизмами реализации биологической активности витамина, однако уже в 1953 г. круг ферментов, зависящих от присутствия ТДФ, был расширен за счет транскетолазы, а совсем недавно и специфической декарбоксилазы γ-окси-α-кетоглютаровой кислоты. Нет оснований думать, что перечисленным исчерпывается перспектива дальнейшего изучения витамина, так как эксперименты на животных, данные, получаемые в клинике при лечебном применении витамина, анализ фактов, иллюстрирующих известную нейро- и кардиотропность тиамина, с несомненностью указывает на наличие еще каких-то специфических связей витамина с другими биохимическими и физиологическими механизмами (В. Б. Спиричев, 1966; Ю. М. Островский, 1971).
2. Химические и физические свойства витамина В1
Тиамин (В. М. Березовский, 1959; В. А. Девятнин, 1964), или 4-метил-5-β-оксиэтил-N- (2-метил-4-амино-5-метилпиримидил) -тиазолий, получается синтетически обычно в виде хлористо-или бромистоводородной соли:
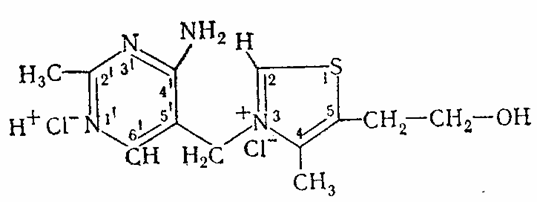
-Рйаминхлорид (М-337,27) кристаллизуется с ½ Н2О в бесцветных моноклинических иглах, плавится при 233—234° (с разложением). В нейтральной среде его спектр поглощения имеет два максимума — 235 и 267 нм, а при рН 6,5 Один — 245—247 нм. Витамин хорошо растворяется в вода и уксусной кислоте, несколько хуже в этиловом и метиловом спиртах и нерастворим в хлороформе, эфире, бензоле, ацетоне. Из водных растворов тиамин может быть осажден фосфорно-вольфра-мовой или пикриновой кислотой. В щелочной среде тиамин подвергается многочисленным превращениям (Metzler, 1960), которые, в зависимости от природы добавленного окислителя, могут завершаться образованием тиаминдисульфида (X) или тиохрома (IX).
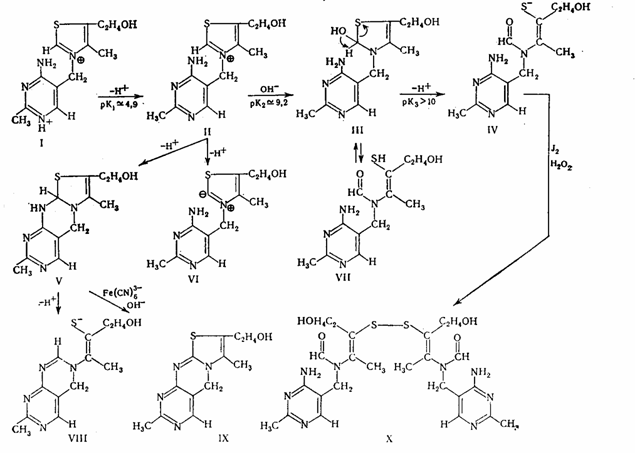
В кислой среде витамин разлагается только при длительном нагревании, образуя 5-гидрокси-метилпиримидин, муравьиную кислоту, 5-аминометилпиримидин, тиазоловый компонент витамина и З-ацетил-3-меркапто-1-пропанол. Среди продуктов распада витамина в щелочной среде идентифицированы тиотиамин, сероводород, пиримидодиазепин и др. Получены также сульфат и мононитрат витамина. Известны соли тиамина с нафталенсульфоновой, арилсульфоновой, цетилсерной и эфиры с уксусной, пропионовой, масляной, бензойной и другими кислотами.
Особое значение имеют эфиры тиамина с фосфорной кислотой, в частности ТДФ, являющийся коферментной формой витамина. Получены (Fragner, 1965; Schellenberger, 1967) гомологи тиамина путем различных замещений у второго (этил-, бутил-, оксиметил-, оксиэтил-, фенил-, оксифенил-, бензил-, тиоалкил-), четвертого (окситиамин) и шестого (метил-, этил) атомов углерода пиримидина метилированием аминогруппьь, замещением тиазоловогоинхла на пиридиновой (пиритиамин), имидозоловый или оксазфювый, модификациями заместителей у пятого углерода тиазола (метил-, оксиметил-, этил-, хлорэтил-, оксипропил- и др.). Отдельную большую группу соединений витамина составляют S-алкильные и дисульфидные производные (Matsukawa e. а., 1970). Среди последних наибольшее распространение как витаминный препарат получил тиаминпропилдисульфид (ТПДС).
3. Распространение витамина В1, в природе.
Тиамин распространен повсеместно и обнаруживается у разных представителей живой природы (Р. В. Чаговец и др., 1968). Как правило, количество его в растениях и микроорганизмах достигает величин значительно более высоких, чем у животных. Кроме того, в первом случае витамин представлен преимущественно свободной, а во втором — фосфорилированной формой. Содержание тиамина в основных продуктах питания колеблется в довольно широких пределах в зависимости от места и способа получения исходного сырья, характера технологической обработки полупродуктов и т. п. Величины, приводимые по этому поводу в литературе (Ф. Е. Будагян, 1961; В. В. Ефремов, 1969; П. И. Шилов, Т. Н. Яковлев, 1964), характеризуют, как правило, уровень витамина до кулинарной обработки, которая сама по себе значительно разрушает тиамин. В среднем можно читать, что обычное приготовление пищи разрушает около 30% витамина. Некоторые виды обработки (высокая температура, повышенное давление и наличие больших количеств глюкозы), разрушают до 704-90% витамина, а консервация продуктов путем обработки их сульфитом может полностью инактивировать витамин В злаковых семенах других растений тиамин, подобно большинству водорастворимых витаминов, содержится в оболочке и зародыше. Переработка растительного сырья (удаление отрубей) всегда сопровождается резким снижением уровня витамина в полученном продукте. Шлифованный рис, например, совсем не содержит витамина.
Содержание тиамина в некоторых продуктах питания (В. В. Ефремов, 1960)
|
Продукт |
Содержание тиамина в мкг % |
Продукт |
Содержание тиамина в мкг % |
|
Пшеница |
0,45 |
Томаты |
0,06 |
|
Рожь |
0,41 |
Говядина |
0,10 |
|
Горох |
0,72 |
Баранина |
0,17 |
|
Фасоль |
0,54 |
Свинина |
0,25 |
|
Kpупa овсяная |
0,50 |
Телятина |
0,23 |
|
>>гречневая |
0,51 |
Ветчина |
0,96 |
|
>> манная |
0,10 |
Куры |
0,15 |
|
Рис шлифованный |
0,00 |
Яйца куриные |
0,16 |
|
Макароны |
следы |
Рыба свежая |
0,08 |
|
Мука пшеничная |
0,2—0,45 |
Молоко коровье |
0,05 |
|
>> ржаная |
0,33 |
Фрукты разные |
0,02—0,08 |
|
Хлеб пшеничный |
0,10—0,20 |
Дрожжи пивные сухие |
5,0 |
|
>>ржаной |
0,17 |
Орехи грецкие |
0,48 |
|
Картофель |
0,09 |
» земляные |
0,84 |
|
Капуста белокочанная |
0,08 |
Реферат опубликован: 15/06/2005 (16982 прочтено)